Разделы: Физика, Конкурс «Презентация к уроку»Загрузить презентацию (2. Б). Внимание! Предварительный просмотр слайдов используется исключительно в ознакомительных целях и может не давать представления о всех возможностях презентации. Если вас заинтересовала данная работа, пожалуйста, загрузите полную версию. Метод ведения урока: комбинированный.
Эпиграф урока: Жизнь ставит цели науке; наука освещает. Н. К. Михайловский План урока: I. Оргмомент. II. Работа в группах. III. Обсуждение итогов, монтаж презентации. Рефлексия. V. Домашнее задание (Г.
Я. Мякишев. “Электродинамика” 1. Ход урока- Добрый день! Садитесь. Сегодня наша работа будет происходить по. Задания группам. Природа электрического тока в растворах и. Электролиты. Электролитическая диссоциация.
Опыт Фарадея по электролизу. Закон Фарадея. Вольт – амперная характеристика тока в. ЭДС поляризации. Применение электролиза.
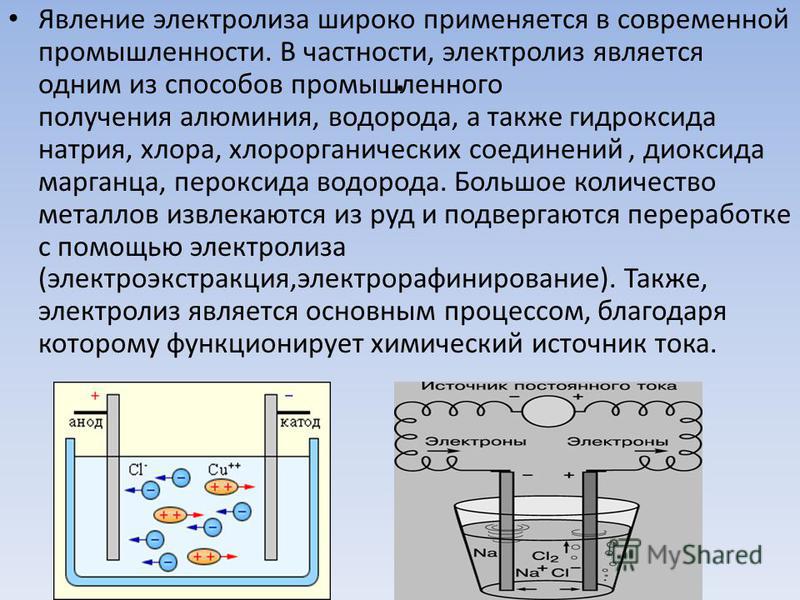
Этот процесс называется электролизом. Закон электролиза. Явление электролиза применяется на практике для получения многих металлов из .
Средства обучения: аудитория: ноутбук, проектор, экран, презентация на .
Содержание задания групп: Электрический ток в электролитах. В. растворах солей, щелочей, кислот происходит. Из- за взаимодействия с полярными.
Положительно заряженными. ОН). Рассмотрим этот процесс на примере бромида. KBr. Взаимодействие атомов брома и калия в молекуле. К+ и отрицательно. Br- . Объясняется это тем, что. При образовании молекулы KBr.

Презентация сформирует представления учащихся о процессе. Презентация к уроку химии «Электролиз расплавов и растворов. Применение. Цели урока: Знать сущность электролиза; Уметь составлять схему электролиза расплавов и растворов электролитов; уметь применять теоретические .

Презентация, предлагается для использования на уроках химии при. ПРИМЕНЕНИЕ ЭЛЕКТРОЛИЗА Презентация выполнена . Тема урока: Электролиз. Законы Электролиз. Применение электролиза. Показать широкий спектр применения электролиза в народном хозяйстве: Способствовать развитию широты взглядов, формированию .
При растворении соли бромида калия в воде. KBr попадают в окружение молекул воды.
В электрическом. поле, создаваемой молекулой KBr, молекулы вды. Часть молекул KBr.
K+ и Br- . Степень диссоциации, т. С увеличением температуры степень. Наряду с процессом диссоциации в растворах. Ионы. разных знаков при встрече могут снова. При неизменных условиях в. При. наступлении динамического равновесия.
Ионная проводимость растворов и. При отсутствии внешнего электрического поля. Если сосуд с раствором электролита включить в.
Положительные ионы, пришедшие к. При этом через раствор. Такую проводимость. В расплавах электролитов.
Жидкие же. металлы обладают электронной проводимостью. Электролиз. При прохождении электрического тока через. Таким образом, на. Процесс выделения на электролитах вещества. В ряде случаев нейтрализуемые на электродах. Эти реакции называют.
Так, например, при электролизе раствора медного. Cu. SO4) на катоде выделяется медь, а.
SO4., который. вступает в реакцию с веществом анода – медью : Cu +. SO4 = Cu. SO4. Благодаря этой реакции концентрация раствора. При постоянной температуре графиком. Эта прямая. не проходит через начало координат, а. Это объясняется тем, что при.
ЭДС. поляризации имеет знак, противоположный знаку. Закон электролиза.
Масса выделившегося вещества равна. Фарадей. Закон электролиза был экспериментально.
М. Фарадеем в. 1. Закон. Фарадея определяет количества первичных. Масса m вещества, выделившегося. Q. прошедшему через электролит: m = k. Q = k. It. Величину k называют электрохимическим.
Масса выделившегося на. Здесь m. 0 и q. 0 – масса и заряд одного иона –. Q. Таким. образом, электрохимический эквивалент k равен.
Так как заряд иона равен произведению. Здесь NA – постоянная Авогадро, M = m. NA – молярная. масса вещества, F = e. NA –постоянная Фарадея. F = e. NA = 9. 64. Кл / моль. Постоянная Фарадея численно равна заряду. Закон Фарадея для.
Технические применения электролиза. Гальваностегия — покрытие металлических. Предмет, подлежащий покрытию. Анодом служит пластинка из того же металла. С рельефного. предмета делают восковый или иной слепок. Рабочая Программа Технология 1 4 Класс Лутцева далее.
Затем. поверхность слепка покрывают тонким слоем. В таком виде. слепок используется в качестве катода, который. Анодом служит медная.
Когда на слепке нарастет достаточно. Остается точная медная копия.
В полиграфической промышленности такие копии. Это позволяет воспроизвести набор в.
Если раньше тираж. Правда, в настоящее время с помощью электролиза. Осаждая металл на длинный цилиндр, получают. Процесс получения отслаиваемых покрытий был. Б. Якоби, который в. Массивные куски. (толстые листы) неочищенной меди, полученной при. Процесс. происходит в больших ваннах с водным раствором.
При электролизе медь анода. Таким же. образом производят рафинирование некоторых. Получение алюминия.
При помощи электролиза получают алюминий. Для. этого подвергают электролизу не растворы солей. В угольные тигли (рис. Аl. 2O3), полученный. Тигель служит катодом. Анодом являются. угольные стержни, вставленные в тигель. Сначала. угольные стержни опускают до соединения с тиглем.
Глинозем при. прохождении тока нагревается и расплавляется. Расплавленный. алюминий, выделяющийся при электролизе. Описанный способ получения алюминия сделал его. Путем электролиза расплавленных солей в. Электролиз используется для гальваностегии.
Молодцы, ребята! Вы отлично справились с. У нас получилась хорошая презентация.